Halogenierte Benzole reagieren mit verdünnter Soda unter hohen Druck- und Temperaturbedingungen zu Phenolen. Diese Reaktion erfordert keine desaktivierenden Gruppen in der ortho/para-Position und folgt einem anderen Mechanismus als die aromatische nucleophile Substitution durch Additions-Eliminierung.
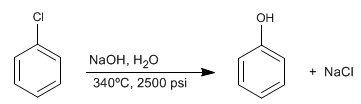
Diese Reaktion wurde 1928 von Chemikern der Dow Chemical Company entdeckt. Der Mechanismus besteht in der Eliminierung von HCl unter Bildung eines instabilen Zwischenprodukts namens Benzin, das von den Hydroxidionen des Mediums angegriffen wird, um Phenol zu bilden.
Stufe 1. HCl-Entfernung
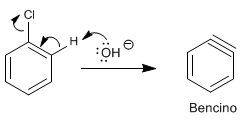
Stufe 2. Zugabe des Hydroxidions zum Benzin
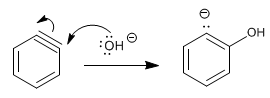
Stufe 3. Protonierung
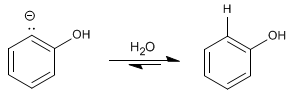
![]() Der Mechanismus dieser Reaktion wird als aromatische nukleophile Eliminierungs-Additions-Substitution bezeichnet.
Der Mechanismus dieser Reaktion wird als aromatische nukleophile Eliminierungs-Additions-Substitution bezeichnet.
Wenn in Benzol Substituenten vorhanden sind, entstehen aufgrund des Angriffs des Nucleophils auf die beiden Kohlenstoffatome der Dreifachbindung Mischungen.