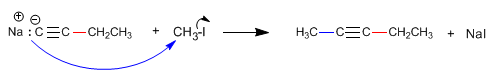
Como vimos en el punto anterior, los alquinos terminales presentan hidrógenos ácidos que pueden ser arrancados por bases fuertes, formando acetiluros (base conjugada del alquino). Los acetiluros son buenos nucleófilos y dan mecanismos de sustitución nucleófila con sustratos primarios.
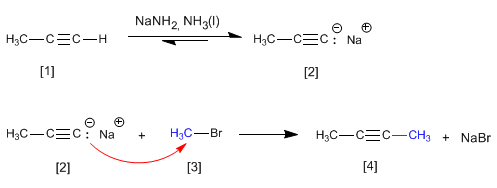
El propino [1] reacciona con amiduro de sodio en amoniaco líquido para formar el propinil sodio [2]. En la segunda etapa el propinil sodio ataca como nucleófilo al bromuro de metilo [3] para formar 2-Butino [4]. En esta reacción el alquino se alquila formándose un enlace carbono carbono que aumenta el tamaño de la cadena carbonada.
La formación de enlaces carbono-carbono es de gran importancia en síntesis orgánica, permitiendo construir moléculas de gran tamaño a partir de otras más pequeñas.
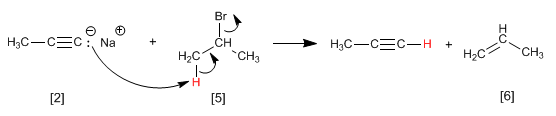
La reacción de alquilación sólo se puede realizar con haloalcanos primarios. Así, el bromuro de isopropilo [5] (sustrato secundario) genera propeno [6] por reacción con propinil sodio [2], mediante mecanismo E2
Ejemplo: Obtener 2-pentino a partir de acetileno
Paso 1. Desprotonación del acetileno con amiduro de sodio
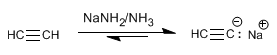
Paso 2. Alquilación con yoduro de etilo
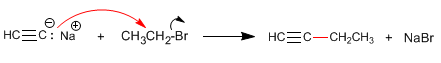
Paso 3. Desprotonación del 1-Butino
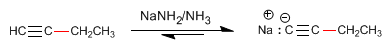
Paso 4. Alquilación del 1-butinil sodio con yoduro de metilo