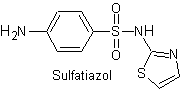
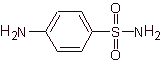
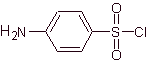
SYNTHÈSE DE SULFAMIDE
On sait que les sulfamides ont été les premiers antimicrobiens à être utilisés par voie systémique. Sa structure chimique est un noyau benzénique avec des groupements amino qui lui confèrent son activité. Le groupe amino est acétylé dans le foie, l'inactivant. Selon le substituant dans ledit secteur, le médicament est plus actif.
Compte tenu de sa similitude avec l'acide para-aminobenzoïque, il se comporte comme un inhibiteur compétitif de cette substance, qui est nécessaire avec la dihydroptéridine pour synthétiser l'acide dihydrofolique, un composé intermédiaire dans la voie de synthèse des folates.
Contrairement aux organismes plus avancés, les bactéries ont besoin de synthétiser leurs propres folates [elles ne les acquièrent pas de l'environnement], donc les sulfamides, en inhibant ce processus, inhibent les processus de synthèse des acides nucléiques et sont BACTÉRIOSTATIQUES.
|
TRIMETROPRIM
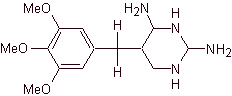
Le triméthoprime est un dérivé des 2,4 diaminopyrimidines telles que |
Ce composé INHIBE l'enzyme dihydrofolate réductase et empêche la formation d'acide tétrahydrofolique, c'est-à-dire qu'ils agissent dans la même voie métabolique que les sulfamides, mais dans une réaction enzymatique ultérieure. Le triméthoprime n'est jamais utilisé seul, mais lorsqu'il est associé à des sulfamides, il est potentialisé de telle manière qu'il devient BACTÉRICIDE, diminue la possibilité de générer des résistances et augmente le spectre antimicrobien. L'association entre sulfaméthoxazole et triméthoprime est fixe : 1:5. Par exemple, les préparations commerciales Cotrimoxazole [forte ou non] viennent avec cette raison. |
Sulfamides, ils sont généralement classés en fonction de la durée de leur action et de la manière dont le médicament est appliqué, ainsi que d'autres caractéristiques. Selon le mode d'action, les sulfamides peuvent être :
pour) Sulfamides à action courte ou intermédiaire.
pour. Sulfamides à usage général
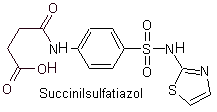
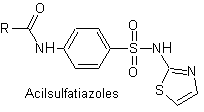
Yo. Sulfathiazole
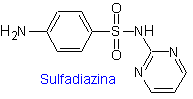
ii. sulfadiazine
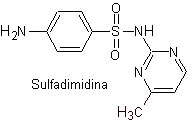
iii. Sulfadimidine
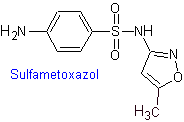
iv. Sulfaméthoxazole (seul ou associé au triméthoprime : cotrimoxazole)
b. Composés très solubles initialement utilisés dans le traitement des infections des voies urinaires.
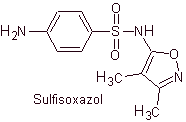
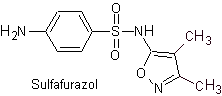
Yo. Sulfisoxazole
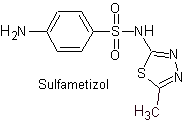
ii. sulfaméthizole
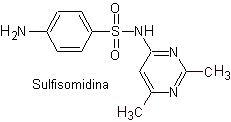
iii. Sulfasomidine
b) Sulfamides à action prolongée.
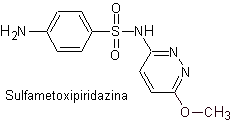
iv. sulfaméthoxypyridazine
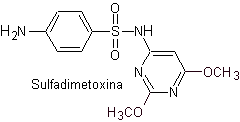
v. sulfadiméthoxine
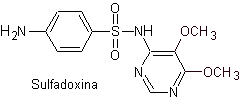
scie. Sulfadoxine
c) Sulfamides limités au tractus gastro-intestinal
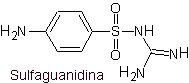
vii. Sulfaguanidine
viii. Sulfatalidine
ix. Sulfasuxidine
X. Sulfazolazine
d) Sulfamides topiques.
xi. acétate de mafénide
xii. sulfadiazine d'argent
xiii. sul facetamide sodique
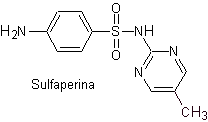
Principaux sulfas :
|
|
……… |
|
|
|
|
|
|
|
…….. |
|
|
|
|
|
|
|
…….. |
|
|
|
|
|
|
|
…….. |
|
|
|
|
|
|
|
|
|
Les structures qui présentent les sulfas présentent généralement deux parties, l'une d'elles est celle correspondant à 4-aminobenzènesulfamide ou chlorure de 4-aminobenzènesulfonique, selon la réaction utilisée pour former le sulfamide, et l'autre partie est généralement un hétérocycle, qui varie bien sûr en fonction du sulfamide particulier en question.
|
4-aminobenzènesulfamide |
…. |
Chlorure de 4-aminobenzènesulfonique |
Synthèse de 4-aminobenzènesulfamide et
Chlorure de 4-aminobenzènesulfonique :
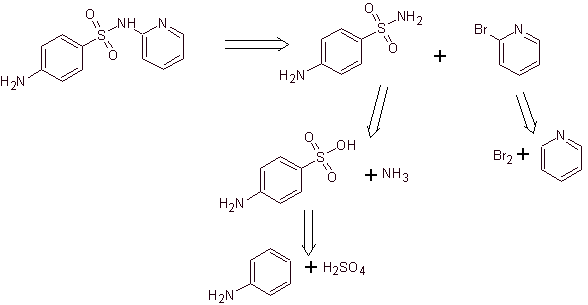
Analyse rétrosynthétique :
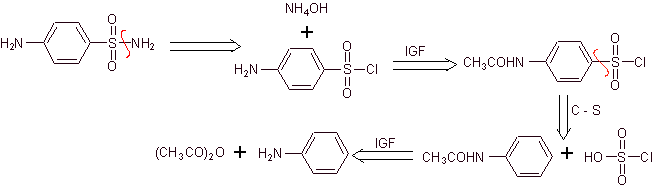
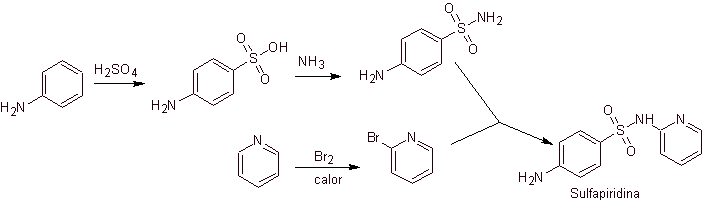
La synthèse:
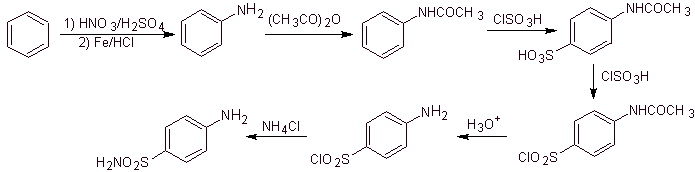
D'autre part, il est également possible de recourir à l'une quelconque des réactions suivantes, pour former les substrats (équivalents synthétiques) : qui sont nécessaires, pour synthétiser les différents sulfamides, selon le cas :
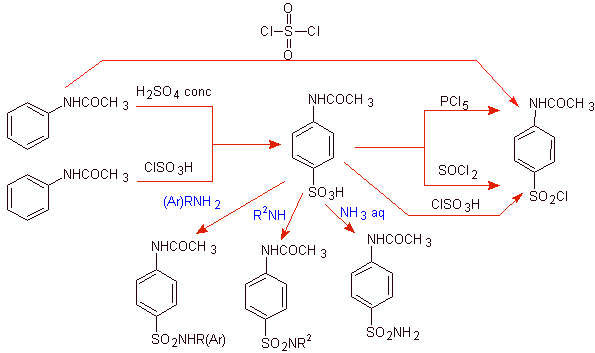
Les aspects de stratégie utilisés de façon récurrente sont liés aux critères suivants :
![]() Le groupe amino de l'aniline est protégé par acylation, pour éviter la formation de l'amide sulfonique, avec les réactifs utilisés pour la sulfonation du benzène : H 2 SO 4 , ClSO 3 H ou SO 2 Cl 2 et
Le groupe amino de l'aniline est protégé par acylation, pour éviter la formation de l'amide sulfonique, avec les réactifs utilisés pour la sulfonation du benzène : H 2 SO 4 , ClSO 3 H ou SO 2 Cl 2 et
![]() Le groupe acétamido de (acétanilide) peut être hydrolysé avant réaction avec l'hétérocycle pour former le sulfa. Alternativement, procéder à une hydrolyse stéréosélective contrôlée, à la fin avec du HCl dilué, car le groupe amide de l'acétanilide est le premier à s'hydrolyser.
Le groupe acétamido de (acétanilide) peut être hydrolysé avant réaction avec l'hétérocycle pour former le sulfa. Alternativement, procéder à une hydrolyse stéréosélective contrôlée, à la fin avec du HCl dilué, car le groupe amide de l'acétanilide est le premier à s'hydrolyser.
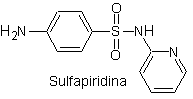
Exemple. Synthétiser la sulfadiazine (MOb 10), le sulfathiazole (MOb 11) et le sulfisoxazole (MOb 12), à partir de matériaux simples et abordables.
MOb 10, Analyse rétrosynthétique. La déconnexion est initiée par la liaison sulfonamide, résultant en deux équivalents synthétiques simples. L'un d'eux est le chlorure de 4-aminobenzènesulfonique, l'autre est la 2-aminopyrimidine, un hétérocycle dont la synthèse n'est pas très difficile.
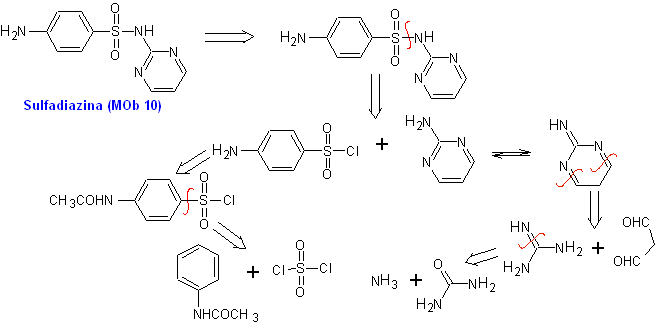
Synthèse de
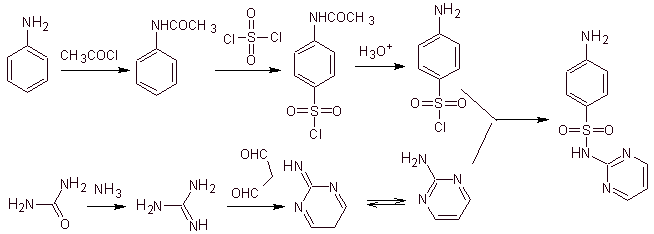
MOb 11. Analyse rétrosynthétique : La déconnexion génère du chlorure de p-aminobenzènesulfonique et l'hétérocycle 2-amino-1,3,thiazole.
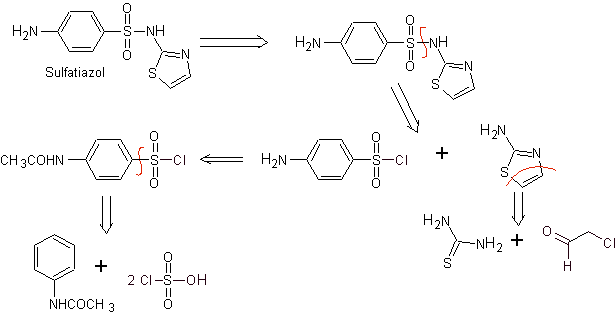
Synthèse de
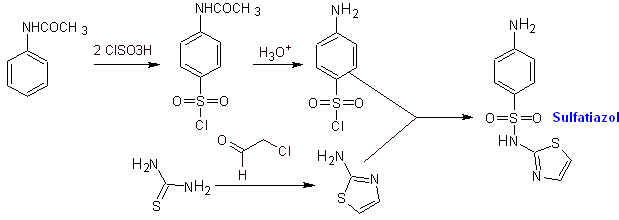
MOb 12. Analyse rétrosynthétique : la déconnexion donne naissance à un nouvel hétérocycle, le 5-amino-3,4-diméthyl-1,2-oxazole
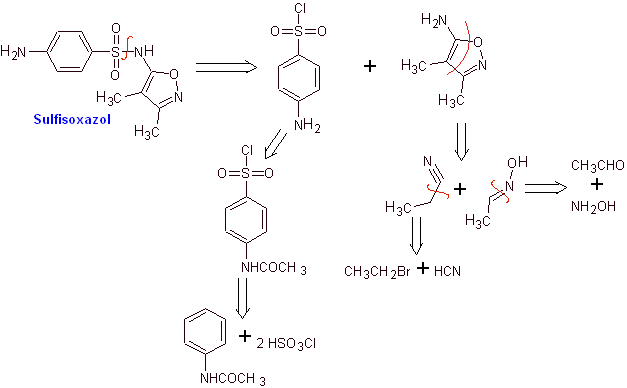
Synthèse de
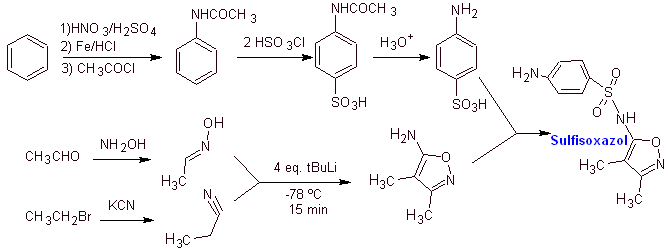
MOb 13. Synthèse de
analyse rétrosynthétique