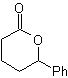
Окисление Байера – Виллигера
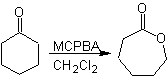
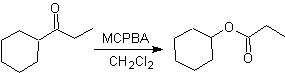
Еще одна реакция, которую можно связать со стратегией Ретросинтез представляет собой окисление кетонов пероксикислотами, более известное как реакция Байера-Виллигера. В циклических кетонах при окислении надкислотами образуются лактоны. Группы, присоединенные к асимметричным кетонам, обладают миграционной способностью, что позволяет буквально «вставить атом кислорода» между карбонильной группой и мигрирующей группой, образуя сложный эфир или лактон.
Следует учитывать, что еноны (α, β ненасыщенные кетоны) не являются хорошими субстратами для окисления Байера-Виллигера, так как алкен гораздо более реакционноспособен, чем кетон. Однако Существуют специальные структуры, в которых алкен может быть защищен ближайшим заместителем из-за стерического эффекта и, таким образом, направить атаку надкислоты на карбонильную группу.
| … |
|
Помните, что миграционная способность различных групп в реакции Байера-Виллигера выглядит следующим образом:
H> Ph> 3° алкил> циклоалкил> 2° алкил> 1° алкил> Me
Предложите схему синтеза следующих молекул:
МОБ 56
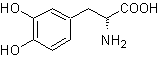
L-допа | . | Моб 57
| . | МОБ 58
|
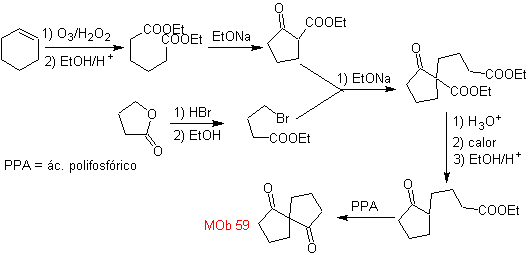
МОБ 59
| МОБ 60
| моб 61
|
МОБ 56. Ретросинтетический анализ.
Альфа-аминокислота
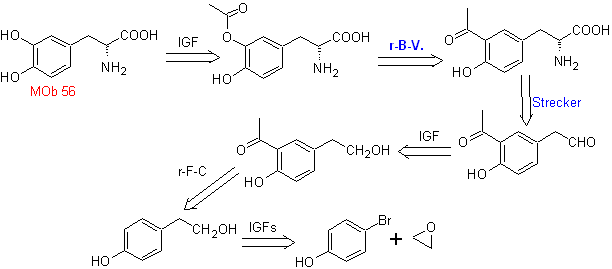
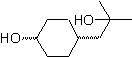
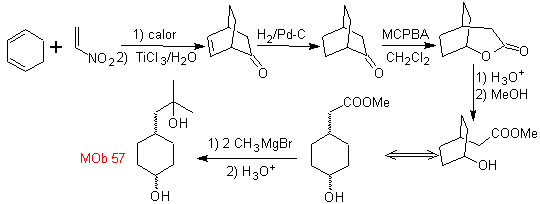
Синтез. Для Для образования необходимого Гриньяра защищают орто-ОН бензола. Синтез Штрекера позволяет получить альфа-аминокислоту, которая окисляется по методу Байера-Виллигера надкислотой и продукт подвергается кислотному гидролизу сложноэфирной группы, что приводит к образованию
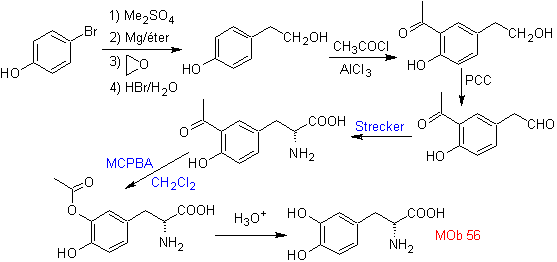
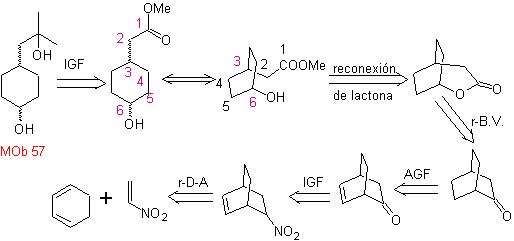
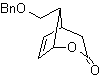
синтез . Он начинается с реакции Дильса-Альдера циклогексадиена и нитроэтилена. Образовавшийся аддукт насыщается, чтобы перейти к окислению Байера-Виллигера. Открытие лактона и этерификация кислотной группы образуют промежуточное соединение, которое затем обрабатывают избытком бромистого метилмагния с получением
МОБ 58. Ретросинтетический анализ. Двойная связь, сопряженная с группой C=O, присутствует в
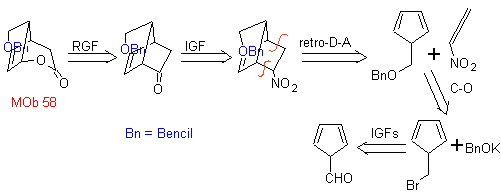
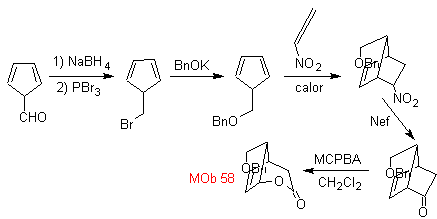
МОБ 59 . Ретросинтетический анализ. Он продолжает отключаться
И снова образуется промежуточный продукт или предшественник 1,3-диСО, который при отсоединении образует новую структуру 1,6-диСО, которую теперь можно повторно соединить, чтобы получить циклогексен в качестве исходного материала.
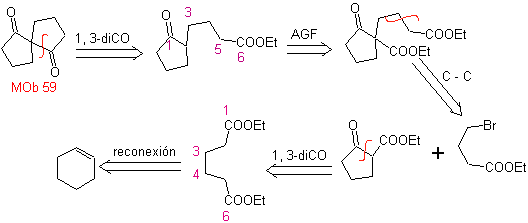
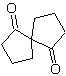
синтез . Окислительное раскрытие циклогексена позволяет получить молекулу-предшественник, которая после реакции с γ-бромэфиром дает молекулу, которая после реакции Дикмана легко превращается в
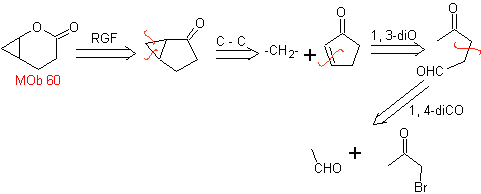
МОБ 60 . Ретросинтетический анализ. Предполагается, что формирование
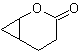
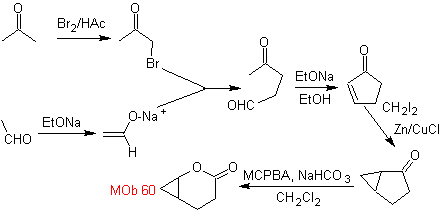
синтез . Енолят ацетальдегида соединяется с α-бромкетоном с образованием молекулы 1,4-диСО, которая в основной среде и этаноле конденсируется с дегидратацией с образованием α,β-ненасыщенного циклопентанона. Реакцию Симонса-Шмидта продолжают образуют циклопропан, а последующее его окисление по Байеру-Виллигеру дает
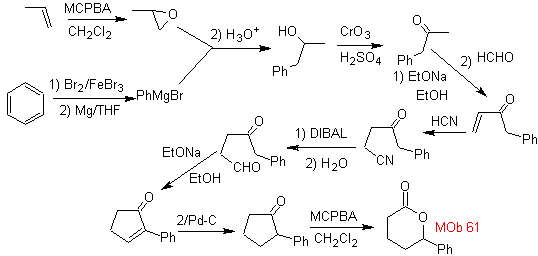
МОБ 61 . Ретросинтетический анализ . Предполагается, что
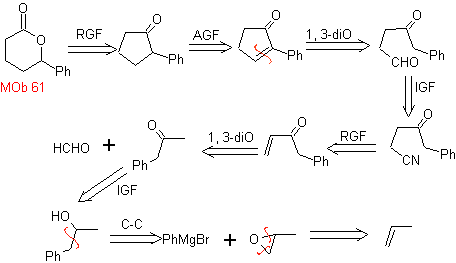
Синтез. Пропен и бензол взяты в качестве исходных материалов, стратегия заключается в восстановлении нитрила до CHO с помощью DIBAL в гексане с образованием промежуточного соединения, которое путем аннелирования Робинсона (или аннелирования) и последующего насыщения обеспечивает адекватный циклопентанон для окисления по реакции Байера. Процедура Виллигера, чтобы сформировать