-
Germán Fernández
-

-
Fuera de línea
-
Administrador
-

-
Mensajes: 2821
-
Gracias recibidas: 751
-
-
|
Hola, la apertura de epóxidos con organometálicos tiene lugar sobre el carbono menos sustituido y requiere de un disolvente aprótico (éter) y atmósfera de nitrógeno. El producto formado es un alcóxido (base del alcohol) que en un segundo paso se protona con agua ácida.
Ambas etapas van por separado, primero la reacción del organometálico en medio éter y después la hidrólisis ácida.
Aprovecho la ocasión para enviarte un saludo y agradecer toda la colaboración que prestas en el foro.
|
|
Por favor, Identificarse o Crear cuenta para unirse a la conversación.
|
-
badman
-
 Autor del tema Autor del tema
-
Fuera de línea
-
Moderador
-

-
Mensajes: 397
-
Gracias recibidas: 47
-
-
|
Hola German,
Si eso lo entiendo pero si te fijas bien, mi pregunta va como hacerlo si quiero introducirlo en el lado mas sustituido.
Si te fijas bien dibuje cuatro posibilidades entiendo 3 la cuarta tal vez no se pueda o yo la desconozco.
Tal vez me esprese mal.
Por otro lado el que esta agradecido al foro soy yo que me hace disfrutar muchisimo y al mismo tiempo aprender.
Saludos
|
|
Por favor, Identificarse o Crear cuenta para unirse a la conversación.
|
-
Germán Fernández
-

-
Fuera de línea
-
Administrador
-

-
Mensajes: 2821
-
Gracias recibidas: 751
-
-
|
No me fijé con suficiente detalle en tu esquema de reacciones. Me temo que no vas a poder atacar con un organometálico al carbono más sustituido de un epóxido, dado que es un nucleófilo bueno y se rige por los impedimentos estéricos.
Una posible solución es abrirlo con HBr, HCl o HI, al trabajar en medio ácido atacan preferentemente al carbono más sustituido. Después puedes formar un organometálico aprovechando ese halógeno (cuprato) y atacar a electrófilos.
En caso de que el alcóxido nos de problemas podemos protegerlo.
¿qué opinas de esta opción?, ¿se te ocurre algo más?
|
|
Por favor, Identificarse o Crear cuenta para unirse a la conversación.
|
-
badman
-
 Autor del tema Autor del tema
-
Fuera de línea
-
Moderador
-

-
Mensajes: 397
-
Gracias recibidas: 47
-
-
|
Hola german,
Si pero eso son dos etapas yo queria hacerlo en una yo estaba pensando mas si era pasibe utilizar un catalizador metalico para que se uniera al par electronico no conpartido del O del epoxido y asi el magnesiano entrar en el mas sustituido.
Pero no se si eso es posible
Saludos
|
|
Por favor, Identificarse o Crear cuenta para unirse a la conversación.
|
-
ccv
-

-
Fuera de línea
-
Sancionado
-

-
Mensajes: 349
-
Gracias recibidas: 192
-
-
|
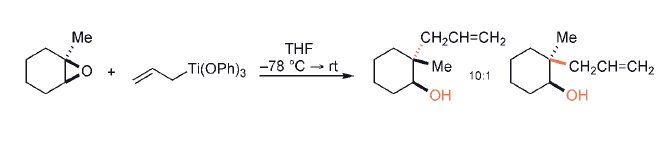
Hola Badman, Germán tiene razón, en general los oragno litiados y Grignard atacan al carbono menos sustituido del epóxido, inclusive en presencia de acidos de Lewis; ya que hay un control esterico que prima sobre la estabilidad del intermediario. Dicho eso, existe una alternativa, que son los reactivos de alilo de titanio que atacan los carbonos más sustituidos dejando un doble enlace muy versátil para trabajar , aquí te dejo un ejemplo.
Referencia: 1) Heterocyclic Chemistry Fifth Edition John A. Joule, pag 593
Saludos 
|
|
Por favor, Identificarse o Crear cuenta para unirse a la conversación.
|
Tiempo de carga de la página: 0.243 segundos