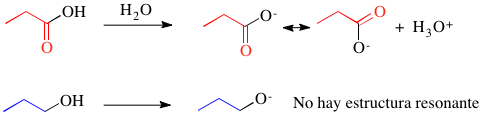
En los ácidos carboxilicos la acidez viene dada por el hidrógeno del grupo alcohol, ahora mi duda es porque un alcohol con la misma cadena R tiene mayor Pka que el ácido carboxilico, cuando tiene el mismo grupo OH.??? ¿¿ porque se disocia mas protones en los ácidos diluidos que un alcohol..??
Pero estuve leyendo un poco mas y encuentro que parte de la respuesta a esto seria que:
El Ac. Carb. es mas ácido porque estabilizan la carga de su base conjugada por resonancia, a comparación del alcohol que solo queda localizada en un solo átomo de O.
Esto lo veo y lo entiendo, pero no entiendo que tiene que ver con el Pka.

Mi análisis es el siguiente, si para determinar el Pka se hace el cociente de la concentraciones de los productos sobre los reactivos,entonces a mi me interesa la [H3O+], osea, la cantidad de protones que se disociaron del reactivo para formar el hidronio, eso es lo que luego por consecuencia determina la [base_conjugada].Por tanto, como influye la carga de la base conjugada si eso no va en el cociente que determina la acidez de la sustancia, Pka.
Muchísimas gracias