Hola, los puntos de fusión son más caprichosos que los de ebullición porque dependen de numerosos factores.
1. Forma de la molécula, las esféricas empaquetan mejor y presentan puntos de ebullición mayores.
2. Fuerzas intermoleculares, los puentes de hidrógeno dan lugar a mayores puntos de ebullición que las fuerzas de London.
3. La masa molecular, una molécula más grande tiende a tener un punto de ebullición mayor que una de menor masa (el tamaño favorece las fuerzas de London).
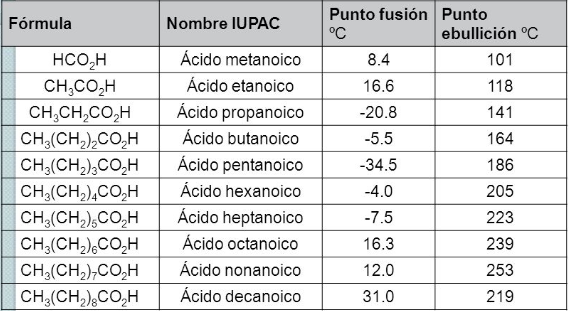
Como puedes observar en la tabla, el ácido metanoico y el etanoico tienen puntos de fusión mayores que los ácidos siguientes, probablemente su mayor simetría esférica les favorece. Propanoico, butanoico, pentanoico empiezan a ser moléculas alargadas.
Al aumentar el tamaño de la cadena, a los puentes de hidrógeno se les suma las fuerzas de London que empiezan a crear una tendencia creciente en los puntos de fusión de ácidos superiores.