-
Noa
-
 Autor del tema Autor del tema
-
Fuera de línea
-
Navegador Iniciado
-

-
Mensajes: 9
-
Gracias recibidas: 0
-
-
|
Buenas tardes, me podrian explicar el mecanismo de la Metanolisis? El ejemplo q tengo es de 1,2-dicloro-4-metilciclohexano en metanol, q sucede y como? Muchas gracias
|
|
Por favor, Identificarse o Crear cuenta para unirse a la conversación.
|
-
Germán Fernández
-

-
Fuera de línea
-
Administrador
-

-
Mensajes: 2815
-
Gracias recibidas: 748
-
-
|
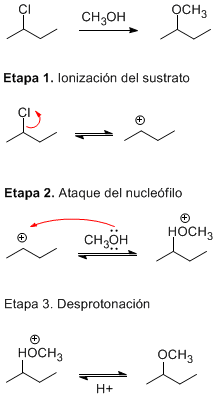
Hola Noa, la metanólisis es la reacción de haloalcanos secundarios y terciaros con metanol. Es decir, un mecanismo S N1
Te indico un ejemplo
El ejemplo que propones es más complejo, puesto que el carbocatión formado queda vecino a un cloro, lo que puede producir una transposición de carbocatión, que generará inevitablente mezcla de productos.
Saludos
|
|
Por favor, Identificarse o Crear cuenta para unirse a la conversación.
|
-
Noa
-
 Autor del tema Autor del tema
-
Fuera de línea
-
Navegador Iniciado
-

-
Mensajes: 9
-
Gracias recibidas: 0
-
-
|
Muchas gracias! Pero perdon la insistencia, te repregunto sobre el ejemplo porq es un ejercicio q no pude resolver en un examen y me qdo la duda jaja...
Si no entendi mal, siempre es un mecanismo SN1, por lo cual si esta en exceso el metanol, se van a unir dos \"metoxis\"?? Se formarian dos carbocationes? O solo una vez se produce el ataque?
|
|
Por favor, Identificarse o Crear cuenta para unirse a la conversación.
|
-
Germán Fernández
-

-
Fuera de línea
-
Administrador
-

-
Mensajes: 2815
-
Gracias recibidas: 748
-
-
|
Al mismo tiempo no deberíamos dibujar dos cargas positivas en la molécula, el intermedio formado es muy inestable. Puede sacar primero un cloro atacando con el metanol y después sacas el segundo cloro.
Este es un mecanismo razonable si no tenemos en cuenta transposiciones.
Saludos
|
|
Por favor, Identificarse o Crear cuenta para unirse a la conversación.
|
-
Noa
-
 Autor del tema Autor del tema
-
Fuera de línea
-
Navegador Iniciado
-

-
Mensajes: 9
-
Gracias recibidas: 0
-
-
|
Si, si, me imaginaba eso mismo ja... Muchisimas gracias!
|
|
Por favor, Identificarse o Crear cuenta para unirse a la conversación.
|
Tiempo de carga de la página: 0.203 segundos