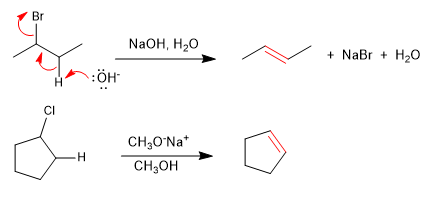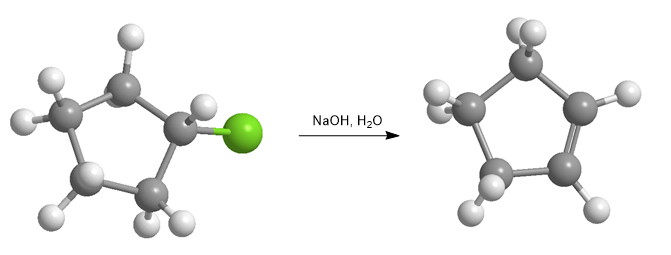
Halogenalkane reagieren mit starken Basen zu Alkenen.
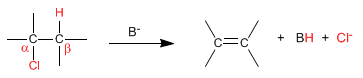
Bei der bimolekularen Eliminierung (E2) entfernt die Base Wasserstoffatome vom Beta-Kohlenstoff und gleichzeitig geht die Abgangsgruppe verloren. Es handelt sich also um eine Elementarreaktion, deren Kinetik zweiter Ordnung ist.
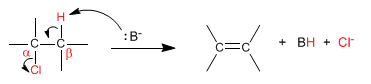
Die Geschwindigkeit der Reaktion hängt von der Konzentration der Base und des Substrats ab.
v = k [Substrat][Basis]
Das Energiediagramm hat folgende Form:
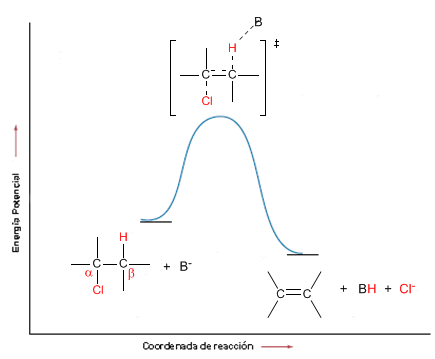
Einige Beispiele für bimolekulare Eliminierungsreaktionen sind: